Естери - Химическа енциклопедия
Естери. заместване продукти от водородните атоми на ОН групите в миньори. или карбоксилна минути за въглеводородни радикали. За да се разграничат полиосновна пълен тон и киселинни естери (например ROSO2 OR 'и ROSO2 ОН, ROCOCH2 COOR' съответно и ROCOCH2 COOH, където R, R '- .. алкил, арил, хетерил ..). Структура етер комплекс може да бъде представен от две резонансни структури:
Етерният част е равнинна или близо до равнинна: единична връзка С - О (структура I) има структура с местоположение tsisoidnym и карбонил двойната връзка на О - Р. дължина връзка на С = О в разлагане. Естери на 0,119-0,122 пМ, С - О 0,131-0,136 нм ъгли CCA 122-126 °, СОС 113-118 °.
Според името на IUPAC за естери, произведени от заглавия. apkilnoy или арил и имената на хидроксилни на отделни компоненти,-ти затваряне чрез заместване "ова" наставка за "съм", например. С2 Н5 COOC2 H5 - пропионат, СН3 OSO2 ОН - метил сулфат. Nek- естери са тривиални имена.
E Фира slozhnye- основният компонент на мазнини. восъци. китова мас; включени в множествено число. етерични масла.
Физични свойства. Естери на долната карбоксилна к-т и прости алкохоли - bestsv. летливи течности. често с приятен плодов аромат; сложни естери на по-висока карбоксилна к-т - bestsv твърди. на островите, почти без мирис. Нисши естери на молец. к-т (alkilsulfity сулфати alkilboraty.) - маслена течност с приятен мирис; сулфати. като се излиза от С9 Н17 - твърдо съединение. Т-RY кипене сложни естери на нисши алкохоли са по-ниски от съответната к-М; Т-RY сулфити кипи обикновено по-ниска от сулфати. Естери на лоша разтворимост. във водата. добър - орг. р-ускорител, които имат средства. диполен момент (5.67 х 10 -30 -6.66 х 10 -30 m Cl х).
IR спектрите на сложни естери присъстват характеристика. ивица при 1750-1700 см -1 (разтягане вибрации на С = О) и 1275-1050 см -1 (разтягане вибрации на С - О). УВ-вия спектър на слаби ивици, наблюдавани при 195-210 пМ преход); dlyanenasysch. естери на силни ивици при 210 нм преход), увеличаване на ненаситеност групата смени на дълги вълни. Химикалът NMR. смяна на 3.7-4.1 т. д. (Н-атом на остатъка алкохол) и 2.2.2 т. д. (Н-атом е киселинен остатък).
Химически свойства. Повечето от естерите на р-ции, свързани с комплекса от нуклеофил. атака карбонил въглероден атом и заместен алкокси.
Хидролизата на сложни естери протича в кисела (молец. To-ти) и в алкална среда [воден или алкохолен р-RY NaOH, КОН, и Ва (ОН) 2. Са (ОН) 2]:
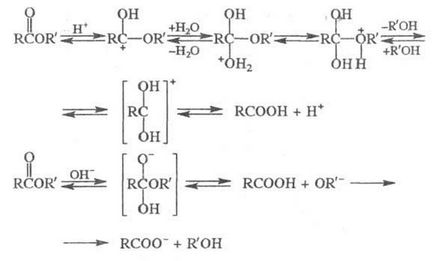
Киселинна хидролиза - обратим процес, алкална -practically необратимо, т.е. карбоксилат анион RCOO а - .. M не се използва .. нападнат от нуклеофил. Скоростта на хидролиза се увеличава с увеличаване на т-тура и с увеличаване на мол. маса етер. Много сложни естери (Ch. Агг. Мазнини) се хидролизират с ензими.
При взаимодействието. сложни естери с алкохоли трансестерификация възниква (виж по-долу). kat.- сух H 2SO 4 или НС1 или алкоксид йон. Амонолиза и аминолиза на естери на комплекс води съответно. RCONH2 на амиди и N-заместени амиди RCONR'R "; катализатори често са NH4 С1 или СН3 OK, р-erator - бензол, диетилов етер или самият амин Nizkomol сложни естери реагират с NH3 при стайна температура ... (за ароматни амини). т-D, vysokomol.- при повишена т-D и налягане. Понякога амонолиза се извършва при ниска т-D да се избегнат странични р-ции, напр.
Особено лесно подвижна vnutrimol. аминолиза; . Например, етерни амини вече циклизират при стайна т-D, като пиролидони:
При взаимодействието. комплекс естер с NH2 ОН за образуване хидроксамова-ви RCONHOH, с хидразин - хидразиди RCONHNH2. с ацетали или въглеродни влакна към тер в присъствие. молец, к-т се обменят р-ТА (вж. ацидолиза).
P-ЛИЗАЦИЯ сложни естери с Гринярдови реактиви, и др. Metalloorg. Кон. да доведе до образуване на третични алкохоли (с изключение fermiatov, притежавани до получаване на вторични алкохоли):
комплекс E Fira влезе в естерна кондензация с връзка. съдържащ активно метилен група (вж. Claisen кондензация), диестери на двуосновен до т претърпяват vnutrimol. кондензация (вж. Dieckmann реакция).
E Фира комплекс формират стабилни карбанйоните и не показва тенденция към себе конденз лесно алкилирани; nek- на такива естери влезе в р-ТА с връзка счупи алкил-кислород, например.
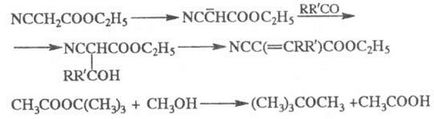
E Фира комплекс миньор. и флуорен-заместен-карбоксилна т алкилира декември Кон. в алкална среда, например.
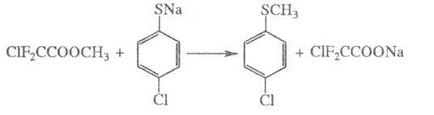
Когато m-D над 300 ° С естери се разлага до образуване на алкени. ацетати пиролиза се провежда в газова фаза при 500-600 ° С:
Бензоати, оксалати и разлага при ниско-ма т в течна фаза.
комплекс E Fira устойчиви на оксидиращи агенти. Възстановяване етер комплекс (Na в етанол. LiAlH4. A1H3 и др.) Води до алдехиди. но обикновено възстановяването продължава - до първичен алкохол: Katalitich. хидриране в присъствието на сложни естери. хромат (III), когато m мед-D 200-300 ° С и налягане от 10-30 МРа - Ind. метод за получаване на алкохоли. Когато възстановяването alifatich естери. моно- и дикарбонова на Na-тон в кипящ ксилол acyloins образуват (вж. Atsiloinovaya кондензация).
Първи. Naib. широко използване естерификация - взаимодействие. алкохоли до-трет: RCOOH + R'OHRCOOR '+ Н2 О. Това - обратим р-ТА, в позиция рояк равновесие зависи от естеството и -VA до-ви и алкохол и равновесната концентрация се характеризира с естерификация продукт (т. наречен. граница етерифициране), например. при равни. съотношение CH 3 COOH и С2 Н5 ОН равновесие се установява, когато
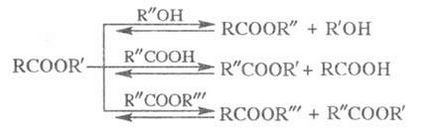
Равновесието е изместена вдясно от дестилиране на алкохол по-колебливи. до-ви или етер. Методът, използван за получаване на естери. притежавани до не може да бъде получено чрез естерификация. напр. винилови или изопропилови естери на по-висок к-т.
Fira Е комплекс също произвежда киселинна алкохолни нитрили (kat.- H 2SO 4 НС1, п-толуенсулфонова киселина ;. P-ЛИЗАЦИЯ 1); алкилиране на карбоксилат анион (к-M, или техни соли) алкилови халиди, алкени в присъствие. катализатори, (2,3); от алдехиди на реакцията Tischenko; метилов естер - р-ТА до тон с диазометан (4); листоминиращи естери. за-т - взаимодействие. последните, както и тяхното galogenangadridov с алкохоли или феноли (5,6) или Miner. к-т с олефини (7):
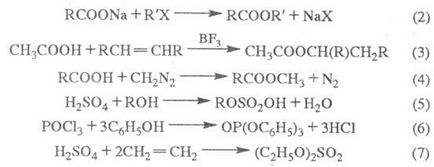
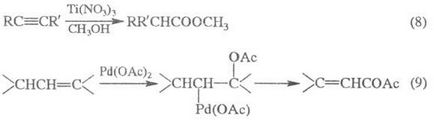
E Fira комплекс дикарбоксилна висока к-т се получава от солите на естери на дикарбоксилни киселини, до-тон в електрохимични условия. р-ТА Колбе:
2ROOC (СН2) п-COONa ROOC (CH2) 2n COOR
E Fira комплекс сярна и фосфорна к-т са оформени в окисление на съответните фосфити и сулфитите.
Определение. За откриване на сложни естери използваха р-ТА с хидроксиламин. генерирани хидроксамова да-ви даде FeS13 характерен червен цвят, за да се определи броя и -kislotnoe летлив номер. и хроматографски техники.
Литература Вейган-Hilgetag, експерименталните методи в органичната химия. на. с него. М. 1968 Общо органичната химия. на. от английски език. Vol. 4, М. 1983, стр. 288-388; Kirk-Othmer енциклопедия, 3 изд. с. 9, N. Y. 1980, стр. 311-37.